Roberto Iotti, Elena Cioni, Antonella Piazza, Elisabetta Catellani, Elisa Gasparini, Valeria Manicardi. SOS di Cardiologia, Dipartimento Internistico, Ospedale di Montecchio Emilia, AUSL di Reggio Emilia.
La Sindrome di Tako-Tsubo è una sindrome cardiaca acuta, identificata agli inizi degli anni ’90 dai ricercatori giapponesi, come una nuova entità clinica, che simula l’infarto miocardico acuto. Altri sinonimi riportati in letteratura sono: “Broken Heart” Syndrome (letteralmente”cuore rotto”), neurogenic myocardial stunning, stress cardiomyopathy, stress-induced cardiomyopathy, ampulla” cardiomyopathy.
La cardiomiopatia esordisce con un quadro clinico del tutto simile a quello di un infarto miocardico acuto (STEMI) o di una sindrome coronaria acuta, in considerazione della sintomatologia, delle tipiche alterazioni elettrocardiografiche ed ecocardiografiche oltre che delle alterazioni biochimiche rilevate.
Tale patologia sembra correlata a stress psichici intensi (14-38%) (forti emozioni, paura, panico, spaventi, lutti), e fisici (17-77%), con prevalenza nel sesso femminile (95%) in post menopausa (58-70anni) (1-8).
Alcuni Autori hanno proposto di ricondurre tale “nuova” entità clinica all’antica credenza popolare costituita dalla sindrome del “crepacor” che tanto si confonde comunque con possibili e forse più frequenti infarti miocardici acuti o eventi aritmici maligni.
Elementi diagnostici
L’elettrocardiogramma in fase acuta mostra spesso un’onda di lesione (sopraslivellamento del tratto ST) tipica dell’infarto miocardico acuto o meno frequentemente T negative (espressione di sofferenza ischemica miocardica). L’evoluzione ECGgrafica può essere Q o più frequentemente non Q con onde T negative giganti espressione di ischemia diffusa.
Dal punto di vista biochimico vi è un incremento come nell’infarto miocardico acuto (anche se spesso ben più modesto), degli indici di miocardiocitonecrosi, con un innalzamento degli enzimi cardiaci (“troponina”, “mioglobina” e “CK massa”), espressione di danno miocardico acuto.
Gli esami strumentali (Ecocolordoppler Cardiaco) evidenziano una estesa acinesia con atteggiamento espansivo-aneurismatico “ballooning” a livello delle porzioni medio/apicali del ventricolo sinistro; nei segmenti basali è presente ipercinesia compensatoria.
La diagnostica invasiva (Coronarografia) imprescindibile per porre una diagnosi corretta e differenziale con l’IMA, permette di escludere lesioni coronariche epicardiche significative.
Il nome deriva dal fatto che la forma che il ventricolo sinistro, all’esame ecocardiografico ed alla ventricolografia (in quest’ultima forse ancor più marcata) (figura 1) ricorda la trappola per polpi, (“tako=polipo; tsubo=cestell “) usata un tempo in Giappone (1-8) (figura 2).
La diagnosi della Sindrome di Tako-Tsubo può essere effettuata solo dopo aver escluso:
- IMA con coronaropatia sottostante.
- Sindrome Coronarica Acuta.
- Miocardite, pericardite.
- Dissezione aortica.
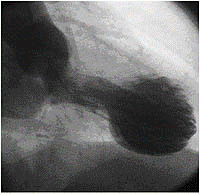
Figura 1: Ventricolografia : tipico aspetto dell’”apical ballooning” (aspetto a palla) del Vsn.

Figura 2 “Takotsubo”
L’aspetto che il ventricolo sinistro assume (tako-tsubo shape ) è dovuta ad un “completo” esaurimento dell’attività muscolare cardiaca (myocardial stunning) una sorta di “stordimento” o paralisi, delle porzioni medie ed apicali del cuore con ipercinesia compensatoria dei segmenti basali (1-5).
Naturalmente l’aspetto più interessante e peculiare è rappresentato dal fatto che si manifesti in individui con rischio cardiovascolare basso (dimostrato dall’assenza di significative stenosi a livello dell’albero coronario). Uno studio francese del gennaio 2006, ha evidenziato come i casi studiati dal 2001 riguardano quasi esclusivamente donne sessantenni, in post-menopausa, con problemi di depressione o ansia (il 50% delle pazienti del campione francese fa uso di ansiolitici).
Il rischio di questa malattia è rappresentato dalle eventuali ricadute (17,7%), soprattutto nei casi associati a depressione o ansia (8).
Fattori predisponenti
I “trigger” responsabili dell’”apical ballooning” (aspetto a palla) includono pertanto stress emozionali ed esacerbazione di disordini sistemici preesistenti (accidenti cerebrovascolari, addome acuto, distress respiratori) e le donne, come accennato, sono colpite da 6 a 12 volte più degli uomini. La mortalità ospedaliera è dell’1,1% (range 0,4-3%) e solitamente il ventricolo recupera la sua piena funzionalità entro 2-4 settimane (6).
La “tako-tsubo ” sindrome rappresenta l’1-2% degli ingressi per sospetto infarto miocardico acuto in Giappone nel corso dell’ultima decade; in uno studio condotto negli USA nel 2002-’03 è stata riportata un’incidenza del 2,2% dei pazienti ricoverati per STEMI (7).
Caratteristica positiva di tale patologia è la sua rapida e completa risoluzione dopo che all’esordio si manifesta con una importante disfunzione ventricolare sinistra.
Eziopatogenesi
Nella genesi di tale entità clinica, sembrava che vi fosse il vasospasmo coronarico epicardico talora anche di più rami coronarici contemporaneamente (nei primi studi dimostrato angiograficamente in percentuali anche del 22%). La combinazione infatti di flusso rallentato (TIMI<2) alla coronarografia e l’assenza di lesioni critiche o placche ateromasiche complicate nelle coronarie epicardiche riconduceva e deponeva per un’alterazione importante del microcircolo; tale ipotesi sebbene nei primi studi era stata esclusa (valutando la riserva di flusso con Doppler Wire non furono riscontrate alterazioni compatibili con microcircolo”danneggiato”) e collegata alla disfunzione meccanica secondaria alla discinesia dei segmenti del ventricolo sinistro interessati è stata recentemente smentita.
Lo studio di L.Galiuto et al. ha dimostrato come il più probabile meccanismo fisiopatologico della sindrome sia una vasocostrizione reversibile “multiterritoriale” del microcircolo coronarico. I ricercatori ,in tale studio, hanno osservato che infondendo adenosina, si otteneva un temporaneo decremento delle alterazioni-anormalità distrettuali della cinetica ventricolare sinistra “Wall motion score index”/ “Wall motion defet lengt” (modesta riduzione in fase acuta e netto miglioramento a 1 mese sia del Left Ventrucolar end diastolic volume che del Left Ventricolar end –systolic volume; importante incremento della frazione di eirzione) con immediato ritorno alle condizioni basali non appena cessava l’infusione della stessa adenosina. Questi risultati sono stati dimostrati soltanto in pazienti affetti dalla sindrome (ABS) ma non nei pazienti colpiti da STEMI (10).
I risultati di tale studio, dimostrando che alla base della disfunzione transitoria ventricolo sinistro vi sia la vasocostrizione del microcircolo coronarico, ha indotto ulteriori trials randomizzati sui potenziali agenti terapeutici ovvero vasodilatatori del microcircolo coronarico come bloccanti canali del calcio, antagonisti dell’endotelina e l’adenosina (10).
Un eccessivo incremento dell’attività “simpatica” (produzione di adrenalina e noradrenalina ) così come una carenza del tasso estrogenico, potrebbe generare dolore toracico, stordimento miocardico, con insufficienza cardiaca fino a quadri di edema polmonare o addirittura shock cardiogeno (4,2%) o fibrillazione ventricolare (1,5%) (7-9).
Recentemente un gruppo di Autori della Mayo Clinic ha proposto un sistema per diagnosticare la malattia basato su 4 punti (6).
- Acinesia o discinesia transitoria dell’apice ventricolare sinistra con esclusione dei segmenti basali
- Assenza di malattia coronaria critica o di rottura acuta di placca preesistente
- Alterazioni ECG compatibili con SCA (Sindrome coronarica acuta)
- Assenza di recenti traumi, feocromocitoma, emorragia subaracnoidea, cardiomiopatia ipertrofica.
1° CASO CLINICO
- Anamnesi cardiologica muta.
- Nessuna terapia cronica domiciliare.
- Recente lutto familiare (madre deceduta da 1 settimana).
- Durante l’attività sportiva aerobica (nuoto) comparsa di dolore oppressivo retrosternale irradiato alla spalla sinistra a carattere crescente d’intensità (5/10), associato a modesta dispnea.
Giunta in visita Cardiologia urgente dopo 3 ore dall’insorgenza della sintomatologia:
- Esame Obbiettivo: Eupnea,toni cardiaci ritmici, validi, soffio sistolico 1/6 puntale, murmure vescicolare presente su tutti i campi polmonari, non stasi né rumori aggiunti polmonari, non edemi declivi. Addome trattabile non punti dolenti.
- Pressione arteriosa 120/70mmHg, Saturazione 02 in aria ambiente 98%.
- ECG: ritmo sinusale, frequenza cardiaca 88 b/min, ST sopraslivellato di 0,5 mm in sede laterale alta ed 1 mm anterosettale (V2-V3) con aspetto speculare inferiore (figure 3)
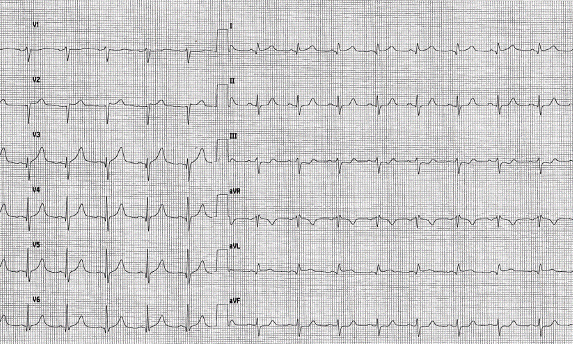
Figura 3
Ecocardio :
Radice aortica nei limiti di norma. Ventricolo sinistro di dimensioni ai limiti superiori (DTD 55 mm), spessori nei limiti, acinesia antero puntale con aspetto globoso “espansivo” omosede, frazione di eiezione del 35%. Insufficienza mitralica lieve e sezioni destre ai limiti superiori (PAPs 32 mmHg). Pericardio indenne.
Si è disposto lo studio coronarografico in emergenza somministrando e.v: ASA 250 mg, eparina sodica 5000 UI, nitrato a basso dosaggio per valori pressori bassi; inoltre carico orale di 300 mg di clopidogrel.
La coronarografia ha mostrato albero coronarico privo di lesioni significative (figura 4,5,6).
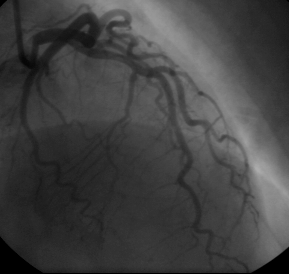
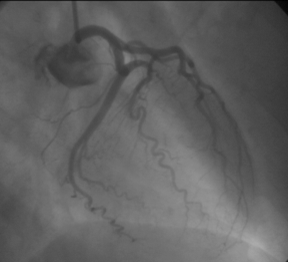
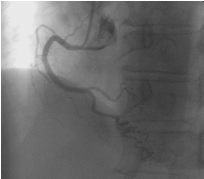 Figura 4, 5, 6
Figura 4, 5, 6
La ventricolografia ha mostrato ancor più l’aspetto aneurismatico anteropuntale con ulteriore riduzione della funzione sistolica (angiograficamente frazione di eiezione < al 30%) (figura 7,8).
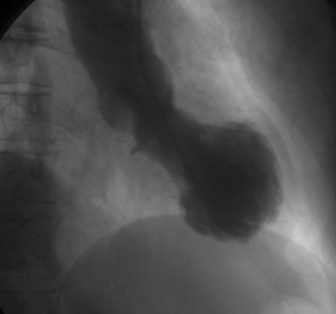
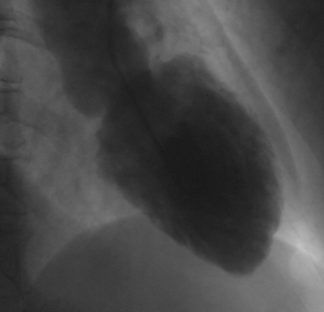 Figura 7,8
Figura 7,8
Successiva evoluzione ECGgrafica in 2 giornata (figura 9).
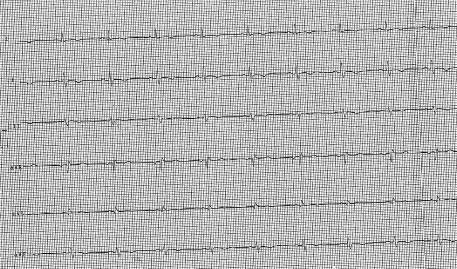
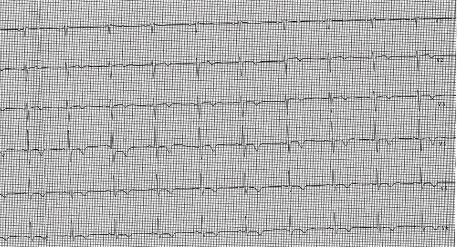 Figura 9. ECG in II giornata
Figura 9. ECG in II giornata
Il decorso clinico è stato privo di complicanze, con buon compenso emodinamico e rapida, precoce mobilizzazione; i valori pressori tendenzialmente bassi hanno consentito soltanto un modesto utilizzo di ace inibitori e betabloccanti oltre alla mono terapia con antiaggregante piastrinico. Il controllo ecocardiografico predimissione ha mostrato in 3°giornata uno straordinario recupero della contrattilità dei segmenti medi e distali con frazione di eiezione del ventricolo sinistro del 55% (persisteva soltanto ipocinesia puntale e scomparsa dell’aspetto aneurismatico).
Al controllo post ricovero, al 1° mese e al 6° mese la paziente era asintomatica e con normalizzazione ECGgrafica.
2° CASO CLINICO
- B.C, 57 anni, sesso femminile .
- Anamnesi cardiologica muta.
- Nessuna terapia cronica domiciliare.
- Recente stress familiare e rilevante stato depressivo.
- Durante attività ordinaria comparsa di dolore gravativo precordiale, a carattere crescente d’intensità (7/10), associato a dispnea e sudorazione algida.
Giunta in visita Cardiologia urgente dopo circa 3 ore dall’insorgenza della sintomatologia:
- Esame Obiettivo. Eupnea ,toni cardiaci ritmici, validi, non soffi auscultabili, Murmure vescicolare presente su tutti i campi polmonari, non stasi né rumori aggiunti polmonari, non edemi declivi.
- Addome trattabile non punti dolenti.
- PA 115/65mmHg, Saturazione 02 in aria ambiente 99%.
- ECG: Ritmo sinusale, diffuso sopraslivellamento ST, e minimo aspetto speculare in aVL (figura 10).
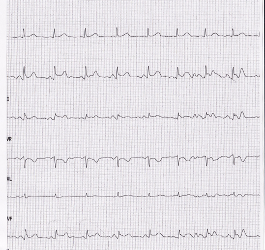
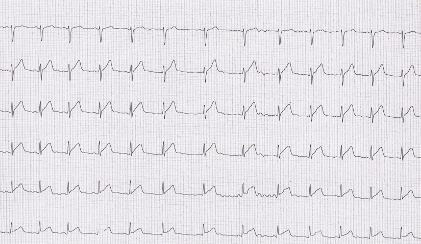
Figura 10
- Tale sopralivellamento è stato transitorio (< 10 min), con rapido ritorno all’isolettrica del tratto ST, già in pronto soccorso con nitrati e.v., con scomparsa dei sintomi.
- L’ecocardio ha mostrato estesa acinesia e rigonfiamento aneurismatico “a pallone” dell’apice del ventricolo sinistro, con ipercinesia compensatoria dei segmenti basali e una frazione di eiezione del 30%.
- L’esame coronarografico ha mostrato coronarie epicardiche indenni da lesioni.
Ventricolografia (figura 11,12)
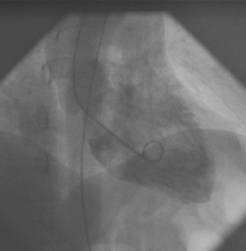
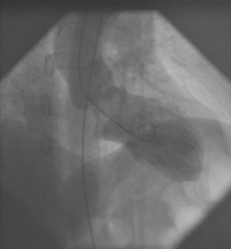
Figura (11,12)
Successiva evoluzione ECGgrafica (non Q) ischemica diffusa in 2 giornata (figura 13).
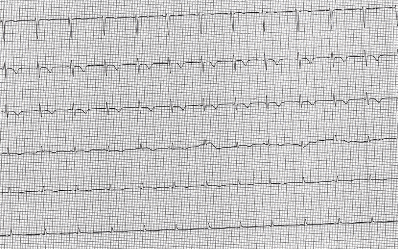
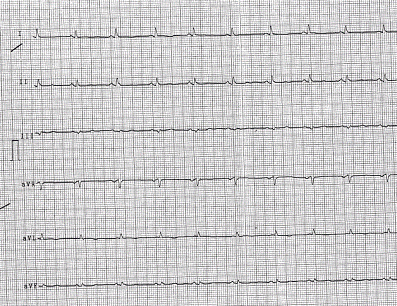 Figura 13 ECG II giornata :
Figura 13 ECG II giornata :
Il decorso anche in questa paziente è stato privo di complicanze sia emodinamiche che aritmiche.
Il controllo post ricovero a 1 mese ha mostrato un quadro clinico stabile con persistenza di modeste alterazioni ischemiche in sede anteriore.
L’ecocardio predimissione in 4°giornata ha mostrato un recupero moderato della frazione di eiezione del ventricolo sinistro 42% con scomparsa anche in questo caso del “ballooning” del ventricolare sinistro.
In seguito circa a 1 mese dopo, la paziente è stata nuovamente ricoverata con un quadro sintomatologico molto più lieve, ECG sostanzialmente immodificato (modesti segni ischemici) con minimo movimento troponinico e senza ulteriori deficit della cinetica ventricolo sinistro apprezzabili ecograficamente.
Abbiamo aggiunto in terapia un calcio antagonista presupponendo il vasospasmo coronarico come eziopatogenesi predominante in questa paziente.
Tale approccio terapeutico si è dimostrato efficace e nei 5 mesi successivi si è ottenuto l’assenza di sintomatologia anginosa e la completa normalizzazione ECGgrafica oltre che un ulteriore miglioramento della funzione sistolica ventricolare sinistra e della frazione di eiezione del 52%.
Conclusioni
Fare una corretta diagnosi di Sindrome di Tako-Tsubo è l’elemento essenziale per il medico che in urgenza accoglie questi pazienti, per evitare l’uso di terapia improprie che potrebbero essere rischiose (ad es.i farmaci trombolitici) o senza alcun beneficio evidente per i pazienti.
Caratteristica peculiare della Sindrome è la regressione rapida e completa in poche settimane. In alcuni casi sono possibili recidive (come nel nostro 2° caso), che pesano negativamente soprattutto sul versante psichico.
La diagnosi è prevalentemente di esclusione -albero coronarico integro alla coronarografia -dopo averla sospettata per gli aspetti peculiari all’ecocardiogramma , ma non esistono dati clinici, strumentali e di laboratorio specifici che definiscano tale patologia in fase acuta.
Oltre alla corretta diagnosi, il trattamento è importante perché la sindrome genera una disfunzione ventricolare sinistra grave anche se transitoria, che va affrontata con tutte le armi farmacologiche dello scompenso cardiaco, per evitare le complicanze, sporadiche ma temibili, ed accelerare la completa guarigione.
La coronarografia in urgenza, è l’unico strumento che permette di confermare il sospetto diagnostico e va privilegiata soprattutto in pazienti di sesso femminile, in postmenopausa, con storia di recente stress fisico o psichico, con scarsi fattori di rischio coronarici ed evidenza ecocardiografica di alterazioni della cinesi caratteristiche di questa sindrome. La coronarografia (e l’eventuale PTCA) in urgenza è preferibile alla trombolisi (peraltro ormai utilizzata raramente nella terapia dello STEMI nella rete cardiologica provinciale),perché permette di visualizzare l’anatomia delle coronarie e la dimostrazione precoce della lesione responsabile dell’Infarto miocardico acuto o la sua esclusione, che in questo caso confermerebbe la diagnosi.
La terapia con beta bloccanti e/o calcio antagonisti può essere di scelta nella ipotesi patogenetica di una eccessiva risposta adrenergica e/o vasospasmo a carico del microcircolo coronarico.
La sindrome è probabilmente a tutt’oggi sottostimata sia come incidenza che prevalenza (i 2 casi clinici descritti sono stati ricoverati nella stessa settimana), ma per riconoscerla deve necessariamente entrare nelle possibili diagnosi differenziali del dolore toracico .
Bibliografia
1) Dec GW. Recognition of the Apical balloning Syndrome in the United States. Circulation 2005; 111: 288-389.
2) Satoh H, Tateishi H, Uchida T, Dote K, Ishihara M. Stunned myocardium with specific tsubo-type left ventricolographic configuration due to multi vessel spasm. In Clinical aspects of myocardial injury: From ischemia to heart failure.ed. Kodama K, Haze K, Hon M. Tokyo: Kagakuhyouronsya Co, 1990: 56-64.
3) Dote K, Mituda H, Ninomiya M, Okuhara T. Acute reversible catecholamine cardiomyopathy. in Syndrome of. Cardiovascular Disease. In Okada R ed. Tokio, Nihon Rinsho, 1996; 166-9.
4) Kawai S, Suzuki H, Yamaguchi H, Tanaka K, Sawada H, Aizawa T et al. Ampulla cardiomyopathy (‘Tako-tsubo Cardiomyopathy)- reversible left ventricular dysfunction with ST-segment elevation. Jpn Circ J. 2000; 64:156-9.
5) Ibanez B, Navarro F, Cordoba M, M-Alberca P, Farre J. Tako-tsubo transient left apical balloning: is intravascular ultrasound the key to resolve the enigma? Heart 2005; 91:102-4.
6) Akashi YJ, Musha H, Nakazawa K, Miyake F. Plasma brain natriuretic peptide intako-tsubo cardiomyopathy. QJM 2004; 97:599-607.
7) Gianni M, Dentali F, Grandi AM, Sumner G, Hiralal R, Lonn E. Apical ballooning syndrome or tako-tsubo cardiomyopathy: a systematic review. Eur Heart J. 2006; 27:1523-29.
8) Bybee KA, Kara T, Prasad A, Lerman A, Barsness GW, Wright RS, Rihal CS. Transient left ventricular apical ballooning: a syndrome that mimicks ST-segment elevation myocardial infarction. Ann Intern Med. 2004; 141:858-65.
9) Abe Y, Kondo M, Matsuoka R, Araki M, Dohyama K, Tanio H. Assessment of clinical features in transient left ventricular apical balloning. J Am Coll Cardiol. 2003; 41:737-42.
10) Galiuto L, De Caterina AR, Porfidia A, Paraggio L, Barchetta S, Locorotondo G et al , Rebuzzi AG, Crea F. Reversible coronary microvascular dysfunction: a common pathogenetic mechanism in Apical Ballooning or Tako-Tsubo Syndrome. Eur.Heart J. 2010; 31:1319-27.
Corrispondenza a
Dott Roberto Iotti
Servizio di Cardiologia
Ospedale Ercole Franchini di Montecchio Emilia
Via Barilla 16 Montecchio Emilia CAP 42027
Email Roberto.iotti@ausl.re.it



Commenti (0)Trackbacks (0)Lascia un commentoTrackback